协会服务
Association Services
随着医疗器械行业发展和法规要求的变化,微粒污染对无菌、植入类器械及初包装材料来讲已经不再是陌生的概念。NMPA发布的《医疗器械生产质量管理规范及ISO13485(2016)标准中都提到了微粒污染。今天小编就跟大家一起来聊聊微粒污染相关的标准及检测要求。
1、《医疗器械生产质量管理规范》
《医疗器械生产质量管理规范附录无菌医疗器械》 2015年101号公告
《医疗器械生产质量管理规范附录植入性医疗器械》 2015年 102号公告
中规定如下:
2.5.2 植入性无菌医疗器械的初包装材料应当适用于所用的灭菌过程或无菌加工的包装要求,并执行相应法规和标准的规定,确保在包装、运输、贮存和使用时不会对产品造成污染。 应当根据产品质量要求确定所采购初包装材料的初始污染菌和微粒污染可接受水平并形成文件,按照文件要求对采购的初包装材料进行进货检验并保持相关记录。 2.7.4 应当根据产品质量要求确定产品的初始污染菌和微粒污染的控制水平并形成文件,明确中间品的存储环境要求和存放时间,按文件要求定期检测并保持相关记录。应当定期对检测记录进行汇总和趋势分析。
2、 ISO 13485(2016)标准
ISO 13485中规定:
6.4.2 污染控制 对于无菌医疗器械,组织应对微生物或微粒物的控制要求形成文件,并保持装配或包装过程所要求的的清洁度。
3、输液输血类产品标准及指导原则
GB 19335/ GB 8368/GB 8369等均提到微粒含量。 《一次性使用输注器具产品注册技术审查指导原则》中明确提出:输液类产品的物理性能中需要包括:微粒污染这一性能。
由于器械材料的复杂性,目前并没有关于微粒可接受的统一标准。现有标准主要有以下几种:
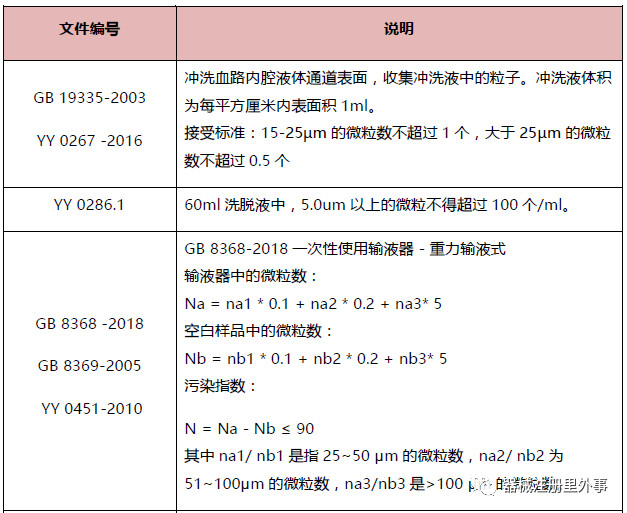

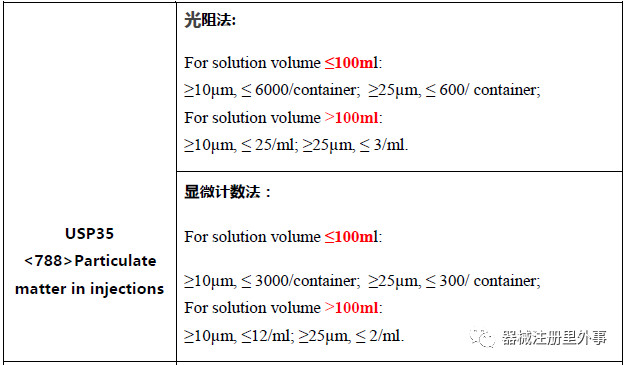

小结
1)中国药典2010版的规定与美国药典(35) 788中的规定一致,但2015版稍微有些改变。
2)理论上目前三类医疗器械均需要监控不溶性微粒。但不是所有的产品都要求在技术要求或出厂检测中开展微粒检测。目前需要控制的都是与血液直接或间接接触类产品:
a. 产品标准中有明确要求的。例如,起搏器、输液输血类血路产品。
b. 产品标准中无明确要求,但产品植入后微粒风险很高 尤其是产品有涂层设计的,需要考虑。如,冠脉类产品。
3)对于产品标准中无明确要求,产品植入后微粒风险不高,一般只需要对原料、半成品、包材、成品建立微粒控制水平即可,不需要在技术要求中规定。
4)对于原材料、包材、半成品等微粒接收标准,可在成品已满足标准要求的基础上,通过对多批次原辅料检测数据的分析建立。
不同产品微粒测试规定的方法不同,但微粒计数的基本原理有两种:显微计数法及光阻法。目前大部分测试均采用光阻法,如光阻法不适合时,再采用显微计数法。目前现有的关于微粒测试一些方法汇总如下:
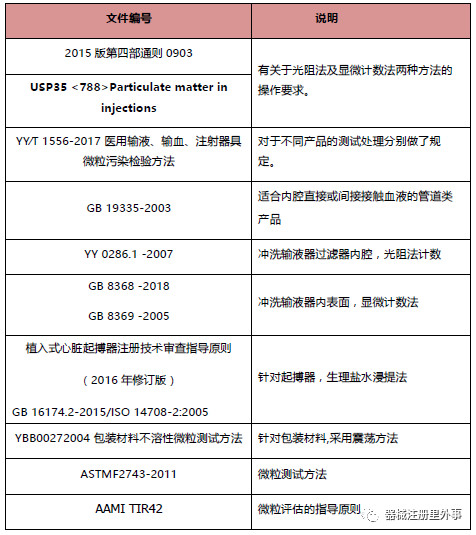
小结
1)考虑到器械产品种类的复杂性,上述提到的测试方法标准仅能作为参考,具体产品的测试方法需要方法学验证后确定。
2)对于不同产品,微粒测试样品的处理需要根据产品特点及临床使用来确定。常见的有:
a.模拟使用法(对于一些血管支架列产品)
b.冲洗法(对一些内腔直接或间接接触血液的管道输液/血类产品)
c.震荡法(对于一些原材料、半成品或包材)
d.生理盐水浸提法(长期植入类产品)
e.长期疲劳法(对于一些有涂层的产品,需要模拟生理场所,长期观察微粒的产品,如支架类产品。)
常见的微粒来源及控制措施如下:
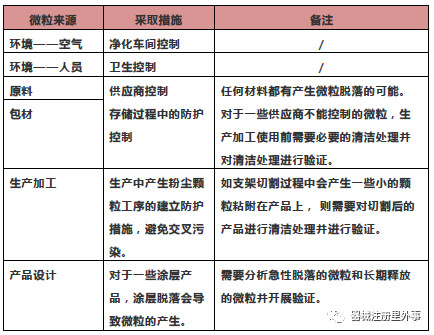
PS: 以上为关于微粒方面的相关分享,如有不合理之处欢迎指正。
微粒污染及控制也是一个小的知识点,但知识在于积累。静下心来认真整理资料的过程中发现需要学习的仍然很多。亦希望本篇分享可以给读到文章的每位一次学习的机会。