协会服务
Association Services
关于举办“2025年医疗器械生产企业管理者代表培训班”
通 知
各有关单位:
医疗器械企业管理者代表在体系运行中担负体系的建立、实施、保持以及持续改进的推进工作,提高整个组织内的法规要求和顾客要求的质量意识等职责。根据医疗器械企业管理者代表管理办法的要求,管理者代表应每年至少参加1次业务培训。新版《医疗器械生产质量管理规范》(修订草案征求意见稿)对医疗器械生产企业管理者代表提出了更高更严格的要求。
为切实提高管理者代表法律法规和业务水平,协会拟定于2025年5月15日至16日举办“2025年医疗器械生产企业管理者代表培训班”。通过本次培训,医疗器械(含 IVD)管理者代表将深入理解并掌握医疗器械相关法规、质量管理体系要求、风险管理知识以及内部审核与管理评审技能,提升质量管理和法规合规能力,确保企业医疗器械产品的质量和安全。现将有关事项通知如下:
一、培训对象
医疗器械生产企业法定代表人、主要负责人、管理者代表、质量管理部门负责人、体系各相关部门负责人及相关人员等。
二、时间及地点
时间:2025年5月15日至16日,上午9:00至下午17:00,共两天,每天早上8:30签到。
地点:厦门市海沧区翁角西路2074号厦门生物医药产业园B13楼一层科技报告厅
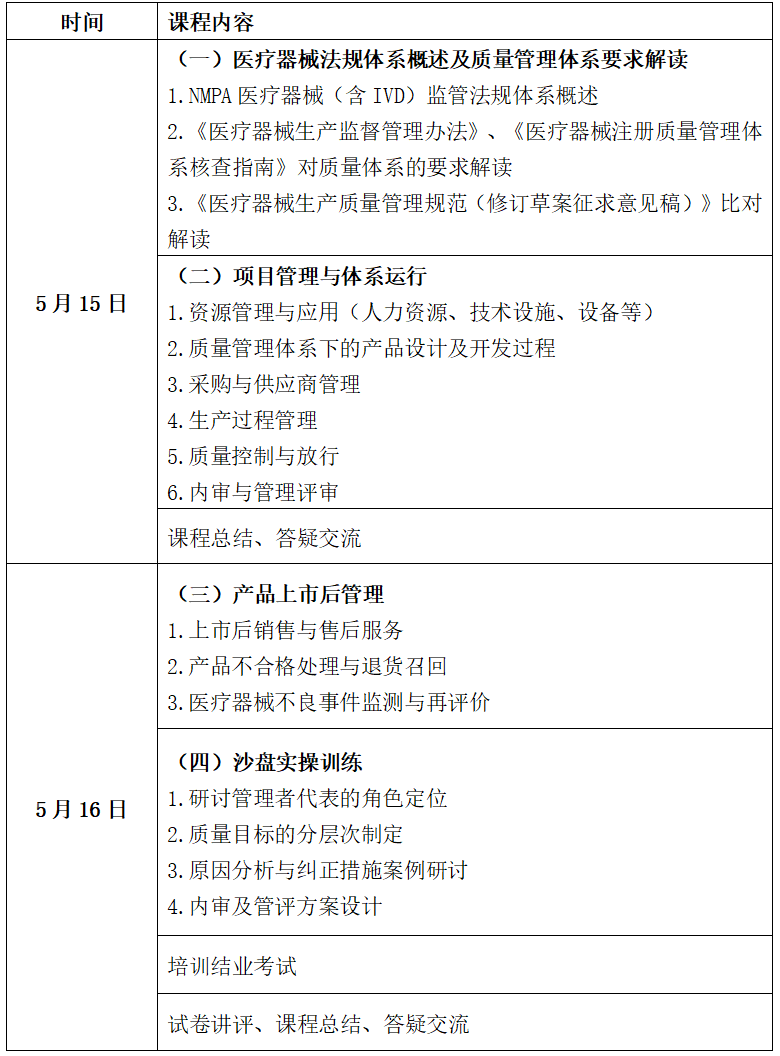
三、日程安排
四、讲师介绍
1.吕懿,北京宝丽永昌医药科技有限公司(丽和康)质量体系部负责人;ISO 13485 及 ISO 9001 主任审核员;10+年医疗器械生产企业工作经历;曾在国内大型医疗器械上市公司就职,担任工艺转化、产品研发、质量工程师等核心岗位,拥有丰富的医疗器械、IVD产品研发经验及生产企业质量体系运行管理经验。
2.冯海俊,北京宝丽永昌医药科技有限公司(丽和康)质量体系项目经理;具有10+年医疗器械生产企业工作经历;曾在国内大型医疗器械上市公司就职,参与IVD产品、三类无源医疗器械、无菌医疗器械的质量管理工作,有多年的质量管理体系实际操作工作经验,并担任公司质量部经理,协助企业完成IVD产品的FDA检查、三类医疗器械的各类型监督检查,具有有丰富的质量管理体系运行经验。
五、收费标准
收费标准:1500元/人(会员)、1800元/人(非会员)(包括培训费、教材费、管理者代表培训合格证书费、午餐费。其它费用自理。)
六、其他注意事项
1、本次培训考试合格,将颁发医疗器械生产企业管理者代表培训合格证书。
2、请各单位于2025年5月13日之前,将报名回执表发至协会邮箱ylqx68@163.com,扫描下方二维码下载报名回执表。

3、汇款方式:报名后,请通过银行汇款转账:
户 名:厦门市医疗器械协会
开户行:工行美仁宫支行
帐 号:4100021309200047971
附注:缴费后请将转账凭证及转账单位的开票信息 (税号)发至协会邮箱予以确认。
4、协会联系方式:
地址:厦门市思明区湖滨四里64号湖光大厦五层D单元
电话: 18950120687、0592-5635883
E-mail:ylqx68@163.com
网址:www.xamd.org
厦门市医疗器械协会
2025年4月16日