
>>>>对发明专利权提出了时限要求
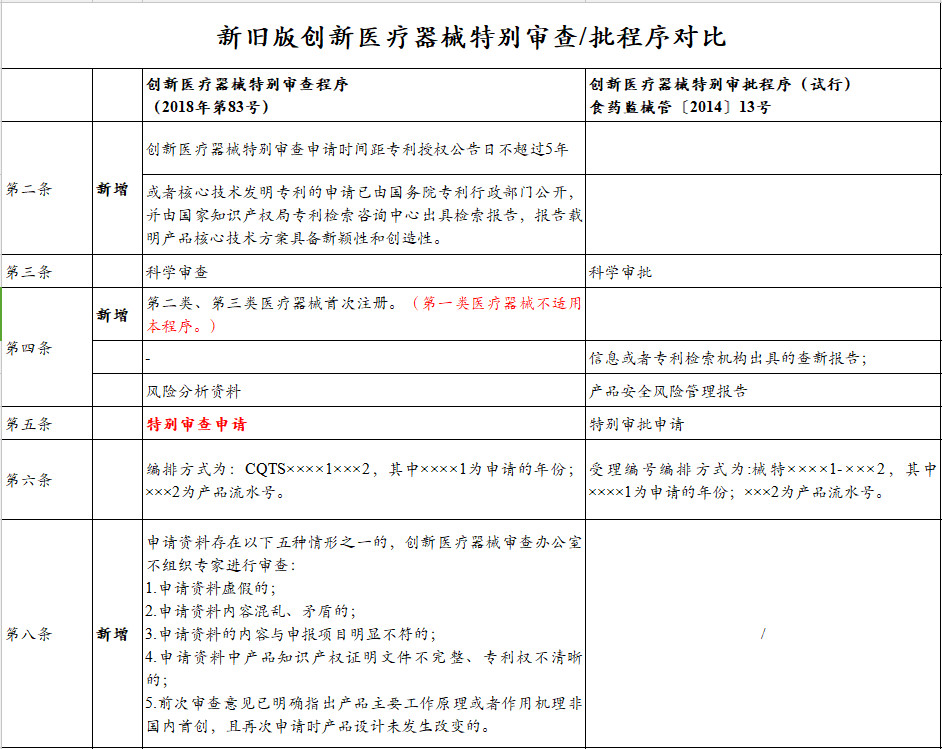
针对已授权的专利:申请人在中国依法拥有产品核心技术发明专利权,或者依法通过受让取得在中国发明专利权或其使用权,创新医疗器械特别审查申请时间距专利授权公告日不超过5年;(主要考虑到专利授权有效期的问题,鼓励创新)
针对未授权的专利:或者核心技术发明专利的申请已由国务院专利行政部门公开,并由国家知识产权局专利检索咨询中心出具检索报告,报告载明产品核心技术方案具备新颖性和创造性。(提及需要由国家知识产权局专利检索咨询中心出具检索报告,2014版的描述则是需要“信息或者专利检索机构出具的查新报告”,字面理解似乎更严格了,只能是国家知识产权局专利检索咨询中心出具检索报告?)
>>>>审查结果不再邮寄纸质通知
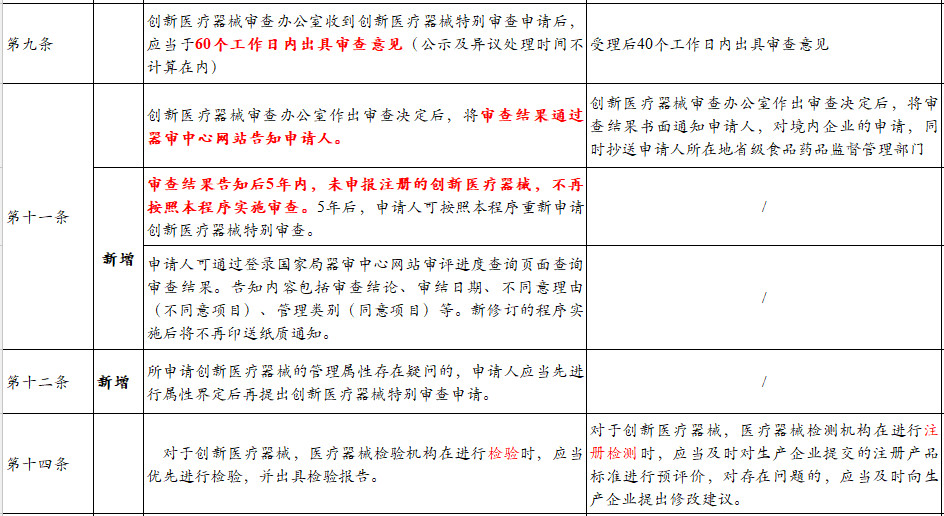
创新医疗器械审查办公室作出审查决定后,将审查结果通过器审中心网站告知申请人。通过登录国家局器审中心网站审评进度查询页面查询。告知内容包括审查结论、审结日期、不同意理由(不同意项目)、管理类别(同意项目)等。
>>>>申请时期及适用范围
申请人申请创新医疗器械特别审查,应当在第二类、第三类医疗器械首次注册申请前。根据《医疗器械监督管理条例》(国务院令第680号),第一类医疗器械实施备案管理,第一类医疗器械不适用本程序。
>>>>通过创新审查后,按照本程序注册时限要求
审查结果告知后5年内,未申报注册的创新医疗器械,不再按照本程序实施审查。5年后,申请人可按照本程序重新申请创新医疗器械特别审查。
>>>>增加了沟通交流途径
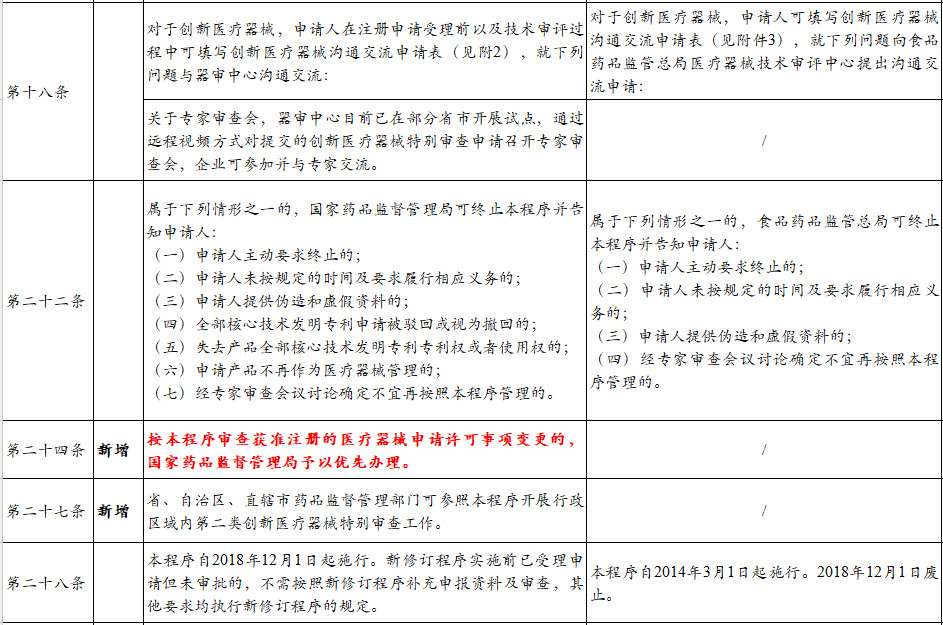
除通过填写创新医疗器械沟通交流申请表申请沟通交流外,国家局器审中心已在部分省市开展试点,通过远程视频方式对提交的创新医疗器械特别审查申请召开专家审查会,企业可参加并与专家交流。(目前江苏、浙江、广东、上海试点已经常态化)
>>>>管理属性存疑的产品
所申请创新医疗器械的管理属性存在疑问的,申请人应当先进行属性界定后再提出创新医疗器械特别审查申请。
>>>>许可事项变更优先
获批后的医疗器械申请许可事项变更,国家药品监督管理局予以优先办理。(终身荣誉)
>>>>不组织专家审查的情形
申请资料存在五种情形之一的,创新医疗器械审查办公室不组织专家进行审查。(存在弄虚作假等问题)
>>>>创新医疗器械审查时限
创新医疗器械审查办公室收到创新医疗器械特别审查申请后,于60个工作日内出具审查意见(公示及异议处理时间不计算在内)。(由原先的40个工作日,调整为现在的60个工作日,申报数量增加导致?)
来源NMPA